本文目录导读:
在生命科学的广袤星空中,CRISPR-Cas9 宛如一颗璀璨新星,以其强大的基因编辑功能照亮了人类对生命本质探索与疾病治疗的新征程,这一技术自问世以来,迅速成为全球科研领域的焦点,引发了一场生物技术的革命,其应用潜力横跨医学、农业、生物研究等多个关键领域,为解决诸多长期困扰人类的难题带来了前所未有的希望与可能。
技术原理
2.1 CRISPR 系统的起源
CRISPR(Clustered Regularly Interspaced Short Palindromic Repeats)本是细菌和古细菌用于抵御外源 DNA 入侵(如噬菌体)的一种天然免疫系统的关键组成部分,当外源 DNA 侵入时,细菌会将其一小段整合到自身 CRISPR 基因座中的间隔序列里,这些间隔序列犹如“黑名单”,记录了曾经遭遇的入侵者信息,而与之相伴的 Cas 蛋白家族则扮演着“卫士”角色,依据这些间隔序列精准识别并切割外源 DNA,保护细菌免受侵害,Cas9 蛋白因其独特的核酸内切酶活性以及相对简便的作用机制,被科学家巧妙改造与利用,开发出了如今广泛应用的 CRISPR-Cas9 基因编辑技术。
2.2 核心组件及其作用
1、Cas9 蛋白:这是一种关键的核酸内切酶,拥有 RuvC1 和 HNH 样核酸酶结构域,分别负责切割目标 DNA 的两条链,从而制造双链断裂,它的功能发挥依赖于向导 RNA 的精准引导以及对靶序列旁特定的原型间隔序列毗邻基序(PAM)的识别,PAM 序列一般为“NGG”,恰似一把特异性“钥匙”,确保 Cas9 蛋白能精确锁定目标 DNA 位点。
2、向导 RNA(gRNA):由 CRISPR 转录而来的 crRNA 与反式激活的 tracrRNA 融合而成,其 5’端约 20nt 的序列可与靶 DNA 反向互补,精准定位待编辑基因;3’端则与 Cas9 蛋白紧密相连,牵引 Cas9 到达目标位置,如同为剪刀精准导航的“指南针”。
2.3 作用机制详解
1、识别与结合阶段:设计合成的 sgRNA 首先与 Cas9 蛋白携手形成复合物,凭借 sgRNA 的引导序列在细胞基因组内地毯式搜索,寻觅与之完全匹配的靶 DNA 序列,一旦发现目标,二者紧密结合,Cas9 蛋白还会对邻近的 PAM 序列进行严格鉴定,唯有两者皆符合条件,才会开启后续切割流程。
2、DNA 切割过程:确认无误后,Cas9 蛋白的核酸酶结构域即刻启动,于 PAM 序列上游第 3 个碱基处果断对 DNA 双链实施切割,造成断裂缺口,这一切割动作犹如精准的“分子手术”,引发细胞内在的 DNA 修复机制。
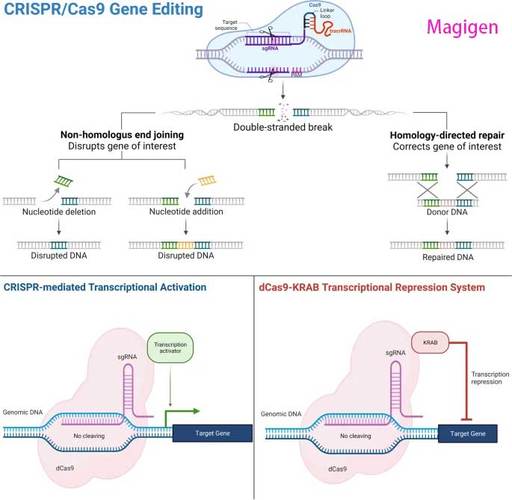
3、修复与编辑结局:细胞主要通过非同源末端连接(NHEJ)和同源重组修复(HDR)两种方式应对 DNA 断裂,若采用 NHEJ 修复,往往会因插入或缺失少数碱基对而导致基因移码突变,致使基因原有功能丧失,达成基因敲除效果;而在存在特定修复模板(含目的基因片段及同源臂)时,细胞会启用 HDR 修复途径,依照模板精确修复断裂 DNA,实现基因敲入或精准替换等定制化编辑。
应用领域
3.1 基础生物学研究
1、解析基因功能:借助 CRISPR-Cas9 轻松敲除、敲入或修饰特定基因,进而细致观测细胞在基因层面变动后的表型变化,深度挖掘基因在细胞增殖、分化、代谢、凋亡等关键生理过程中的核心作用机制,例如在癌细胞研究中,敲除疑似致癌基因后监测肿瘤细胞生长态势,助力揭示癌症发病机理。
2、构建精准动物模型:通过对小鼠、大鼠、斑马鱼等实验动物的受精卵或胚胎干细胞运用 CRISPR-Cas9 编辑技术,培育出携带特定基因突变的动物模型,模拟人类遗传疾病发生情境,像亨廷顿舞蹈症、阿尔茨海默病等神经退行性疾病的动物模型构建,为疾病药物研发与疗效评估筑牢根基。
3.2 医学领域革新
1、攻克遗传性疾病:针对单基因遗传病如镰状细胞贫血、地中海贫血、囊性纤维化等,直接修正患者来源的诱导多能干细胞(iPSCs)或造血干细胞中的致病基因缺陷,再回输至患者体内,从根源上重塑健康细胞功能,以镰状细胞贫血为例,校正血红蛋白基因突变后可望彻底治愈患者,摆脱输血依赖与病痛折磨。
2、癌症免疫疗法进阶:修改 T 细胞的内源性基因,诸如敲除可能诱发免疫排斥反应的基因、嵌入肿瘤特异性抗原受体(CAR)基因,打造靶向性更强、持久有效的 CAR - T 细胞免疫疗法,在血液系统恶性肿瘤治疗成果斐然的基础上,正逐步拓展至实体瘤战场,为癌症晚期患者点燃康复希望之光。
3、传染病防控新思路:理论上可通过编辑人体细胞内与病原体易感相关的基因位点,增强机体对病毒、细菌等病原体的抵抗力,降低感染风险;也可改造蚊虫等传播媒介的基因,抑制病原体在其体内繁殖传播,为公共卫生安全筑起新型防线。
3.3 农业发展助力
1、作物品种改良:精准编辑水稻、小麦、玉米等农作物基因,定向改良产量、品质、抗逆性状,如提升抗倒伏能力、增强抗旱耐盐碱特性、优化籽粒营养成分等,培育满足未来人口增长与多样化饮食需求的高产优质作物品种,夯实粮食安全基石。
2、畜牧业升级:在家畜基因组施加编辑魔法,提高牲畜生长速率、肉质品质、饲料转化率,增强抗病能力,减少养殖成本与疫病损失;还能培育低脂肪、高蛋白等健康特质的新品种畜禽,迎合消费者对营养与口感的追求。
3.4 工业与生物制药腾飞
1、微生物工厂优化:重塑酵母、大肠杆菌等微生物代谢网络,高效生产生物燃料、高附加值化学品、稀缺药物前体等,借由编辑微生物基因调控代谢流,大幅提升目标产物产量与纯度,降低生产成本,推动工业生物技术进步。
2、细胞治疗产品制造:掌控细胞命运,将间充质干细胞精准分化为心肌细胞、神经元等多种功能性细胞类型,用于受损组织器官修复再生;稳定高效生产重组蛋白药物,确保药物质量与供应稳定性,为生物医药产业注入强劲动力。
优势与局限
4.1 显著优势
1、高效精准:能够以极高特异性锚定靶基因位点,极少脱靶现象,确保编辑结果可预测性强,在复杂基因组背景下,仍能准确执行任务,为基因功能精准解析与疾病靶向治疗提供坚实技术保障。
2、操作便捷:相较于传统基因编辑手段,CRISPR-Cas9 系统构建简易,只需依靶基因序列设计合成 sgRNA、搭配 Cas9 蛋白表达载体导入细胞,即可开启编辑之旅,无需繁琐蛋白质工程或复杂克隆步骤,极大节省时间人力成本,加速科研进程。
3、适用广泛:跨越不同生物物种界限,从原核生物大肠杆菌到真核生物动植物细胞、人类细胞,乃至多细胞生物个体水平均可施展编辑身手;兼容多种类型细胞、组织和生物样本,无论是培养细胞株、早期胚胎还是成体器官组织,皆能成为其“用武之地”,彰显强大通用性。
4.2 现存局限
1、脱靶风险隐患:尽管技术持续精进,但脱靶效应难以彻底杜绝,非预期的基因编辑可能引发细胞异常表型、癌变等不良后果,尤其在临床治疗场景下,对患者基因组安全性构成潜在威胁,需高度警惕与深入探究应对之策。
2、编辑效率瓶颈:在某些特殊细胞类型或特异染色体区域,编辑效率不尽人意,受细胞内复杂微环境、染色质状态、基因表达模式等因素制约,部分细胞难以实现高效基因修饰,阻碍技术在特定领域广泛应用脚步。
3、PAM 序列限制:Cas9 蛋白对 PAM 序列依赖度高,自然界中部分基因靶点周边缺乏适配 PAM 序列,致使无法有效招募 Cas9 进行编辑;且 PAM 序列偏好性缩小了可靶向编辑基因范围,一定程度上局限了技术覆盖面。
4、伦理法律挑战:涉及人类生殖细胞编辑时,触及伦理道德红线与敏感社会议题,担忧基因编辑婴儿诞生可能引发人类基因库永久改变、加剧社会不公、催生“设计婴儿”乱象等,促使各国立法谨慎规范该技术应用边界。
发展前景
随着科技日新月异迭代,CRISPR-Cas9 技术正向更高峰攀登,新一代 Cas 蛋白如 Cas12、Cas13
